在醫(yī)療機(jī)構(gòu)中使用���,與本公司生產(chǎn)的一次性使用磁定 位心臟脈沖電場消融導(dǎo)管配合使用�����,用于 治療藥物難治性����、復(fù)發(fā)性���、癥狀性的陣發(fā)性房顫的心臟脈沖電場消融系統(tǒng)�����,在我國屬于第三類醫(yī)療器械注冊(cè)產(chǎn)品�����,且不在免于開展醫(yī)療器械臨床試驗(yàn)?zāi)夸浿畠?nèi)�,本文為大家?guī)硇呐K脈沖電場消融系統(tǒng)臨床試驗(yàn)設(shè)計(jì)實(shí)例,一起看正文�����。
在醫(yī)療機(jī)構(gòu)中使用���,與本公司生產(chǎn)的一次性使用磁定
位心臟脈沖電場消融導(dǎo)管配合使用,用于
治療藥物難治性��、復(fù)發(fā)性��、癥狀性的陣發(fā)性房顫的心臟脈沖電場消融系統(tǒng)���,在我國屬于第三類醫(yī)療器械注冊(cè)產(chǎn)品�����,且不在免于開展醫(yī)療器械臨床試驗(yàn)?zāi)夸浿畠?nèi)�����,本文為大家?guī)?span style="text-wrap: wrap;">心臟脈沖電場消融系統(tǒng)臨床試驗(yàn)設(shè)計(jì)實(shí)例�����,一起看正文�����。
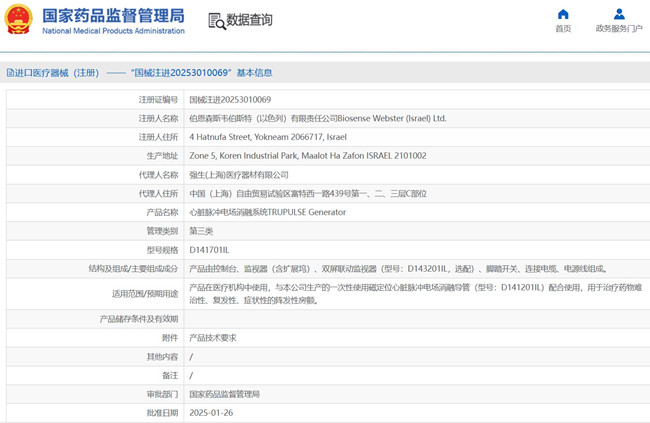
心臟脈沖電場消融系統(tǒng)臨床試驗(yàn)設(shè)計(jì)實(shí)例
醫(yī)療器械臨床試驗(yàn)的目的為評(píng)價(jià)產(chǎn)
品的安全有效性����。臨床試驗(yàn)包括探索性研究和確證性研究,其
中確證性臨床試驗(yàn)的設(shè)計(jì)為前瞻性�����、非隨機(jī)�、多中心、單組目標(biāo)值設(shè)計(jì)����,計(jì)劃入組 248 例受試者。
主要有效性評(píng)價(jià)指標(biāo)為:在有效性評(píng)價(jià)期間(術(shù)后第 91-365
天)���,心電圖數(shù)據(jù)(心電圖(ECG),電話傳輸遠(yuǎn)程心電圖(TTM)或
動(dòng)態(tài)心電圖(Holter))未記錄到持續(xù)≥30 秒的(有癥狀和無癥
狀)快速房性心律失常(房顫�、房速或不明原因的房撲)發(fā)作。
并且無下面失敗模式中的任何一種�����,包括:即刻手術(shù)失敗��,重復(fù)消融失?。瞻灼趦?nèi)大于 1 次重復(fù)消融,在有效性評(píng)價(jià)期內(nèi)任何重復(fù)消融)��,非研究導(dǎo)管使用失?���。ㄊ褂梅茄芯繉?dǎo)管進(jìn)行肺靜脈補(bǔ)點(diǎn)和左房非肺靜脈房顫靶點(diǎn)的治療)�,抗心律失常藥物
(AAD)失敗(使用新的 I 類/III 類 AAD 治療房顫��、房速或不明原因的房撲�����,或服用更高劑量的既往治療失敗的 I 類/III 類
AAD)����,標(biāo)準(zhǔn)12導(dǎo)聯(lián)ECG記錄持續(xù)的房顫/房速/房撲��,以及直流電心臟復(fù)律失敗�����。
主要安全性指標(biāo)為早發(fā)性(消融術(shù)后 7 天內(nèi))主要不良事件的發(fā)生���,包括:死亡(器械相關(guān)或手術(shù)相關(guān)),心房食管瘺�����,
心包填塞/穿孔�,心肌梗死,卒中/腦血管意外�,血栓栓塞,短暫
性腦缺血發(fā)作��,膈神經(jīng)損傷/膈肌麻痹����,心臟傳導(dǎo)阻滯,肺靜脈
狹窄,肺水腫(呼吸功能不全)迷走神經(jīng)損傷/胃輕癱�,心包炎,
重大血管穿刺并發(fā)癥/出血�。其中,房顫消融術(shù)后 90 天內(nèi)出現(xiàn)的心房食管瘺����,房顫消融術(shù)后 30 天內(nèi)出現(xiàn)心包填塞/穿孔���,12 個(gè)月隨訪期間發(fā)生的肺靜脈狹窄及永久性膈神經(jīng)麻痹��,消融手術(shù)
期間或術(shù)后任意時(shí)間發(fā)生的器械或手術(shù)相關(guān)死亡����,均被視為主要不良事件�����。其他安全性終點(diǎn)包括:非預(yù)期器械不良反應(yīng)(UADE)
等�。
次要評(píng)價(jià)指標(biāo)包括:(1) 生活質(zhì)量改善:消融術(shù)后 12 個(gè)月房顫對(duì)生活質(zhì)量評(píng)分的影響��,評(píng)估生活質(zhì)量較基線的改善��;
(2)即刻手術(shù)成功,定義為手術(shù)結(jié)束時(shí)所有確認(rèn)傳入阻滯完成肺靜脈電隔離的受試者百分比��;(3)重復(fù)消融手術(shù)���;(4)有效性評(píng)價(jià)期間(術(shù)后第 91 天-365 天)心電圖數(shù)據(jù)(ECG 或 TTM
或 Holter)未記錄到≥30 秒的(癥狀性和無癥狀)快速房性心
律失常發(fā)作��,但符合以下標(biāo)準(zhǔn)的情況也被視為手術(shù)失?��。涸?3
個(gè)月隨訪訪視窗后服用任何抗心律失常藥物(I 類或 III 類)
治療房顫����;(5)12 個(gè)月單次手術(shù)治療成功;(6)12 個(gè)月臨床成
功����;(7)降低心血管事件住院率:定義為與入組前 6 個(gè)月相比�����,
術(shù)后 12 個(gè)月因心血管事件住院率降低�����;(8)心臟直流電復(fù)律減
少率:定義為與入組前 6 個(gè)月相比��,術(shù)后 12 個(gè)月心臟直流電復(fù)
律率降低;(9)手術(shù)數(shù)據(jù)���,包括:總手術(shù)時(shí)間��、PFA 有效放電
時(shí)間���、標(biāo)測時(shí)間和 PFA 放電次數(shù)、總 X 線透視時(shí)間���、左心房研
究導(dǎo)管停留時(shí)間���;(10)試驗(yàn)用器械使用。
確證性臨床試驗(yàn)實(shí)際入組受試者 277 例���,安全性分析集患者 277 例���,改良意向治療分析集 mITT 274 例,符合方案分析集
PPS 255 例�,在符合方案分析集的患者中,藥物難治性癥狀性復(fù)
發(fā)性陣發(fā)性房顫患者 203 例����。在符合方案分析集的 255 例受試
者中,12 個(gè)月成功率為 74.4%���,精確單側(cè) 97.5%置信下限為
68.5%�����,大于預(yù)先規(guī)定的性能目標(biāo)����。結(jié)果表明該研究符合主要有
效性成功標(biāo)準(zhǔn)���。
符合方案分析集 255 例受試者顯示(1)生活質(zhì)量持續(xù)顯著
改善與基線相比�,12 個(gè)月時(shí)生活質(zhì)量(AFEQT)評(píng)分平均變化
為 32.033 分�;(2)使用研究導(dǎo)管進(jìn)行消融的所有受試者(100%)
均實(shí)現(xiàn)了肺靜脈傳入阻滯,獲得即刻手術(shù)成功�;(3)在符合方
案分析集中,少數(shù)受試者(9%:23/255)在有效評(píng)價(jià)期內(nèi)接受
了重復(fù)消融�����;(4)消融后 12 個(gè)月未記錄到房顫/房速/房撲發(fā)作
且停用 AAD 治療的受試者比例為 70.6%�����;(5)記錄到癥狀性復(fù)
發(fā)的 12 個(gè)月單次手術(shù)治療成功率為 88.2%;(6)消融后 12 個(gè)
月臨床成功的受試者比例為 94.7%���;(7)與基線相比�����,術(shù)后 12
個(gè)月時(shí)因心血管事件住院率降低 100%���。術(shù)后 12 個(gè)月的加拿大
心血管學(xué)會(huì)-房顫的嚴(yán)重程度(CCS-SAF)評(píng)分相對(duì)基線的平均
變化為-2.60,表明生活質(zhì)量改善����。(8)與基線相比,12 個(gè)月時(shí)
直流電復(fù)律發(fā)生率降低 90.7%��;(9)在 277 例導(dǎo)管插入受試者
中���,平均總手術(shù)時(shí)間(±標(biāo)準(zhǔn)差)為 95.14±37.19 分鐘����,平均 PFA有效放電時(shí)間為 17.96±4.67 秒��。平均標(biāo)測時(shí)間為 7.67±5.03 分鐘���,
平均 PFA 有效放電次數(shù)為 74.1± 19.29 次���,平均總 X 線透視時(shí)間
為 9.99±12.20 min,平均左心房研究導(dǎo)管停留時(shí)間為 43.83±18.19
分鐘��;(10)所有受試者都使用試驗(yàn)用器械消融了肺靜脈靶點(diǎn)����。
在 mITT 分析集的 274 名受試者中,未發(fā)生器械或手術(shù)相關(guān)死
亡����、心房食道瘺、心肌梗死��、血栓栓塞�、膈神經(jīng)損傷/膈肌麻痹、
心臟傳導(dǎo)阻滯���、肺靜脈狹窄�����、肺水腫和迷走神經(jīng)損傷/胃輕癱�����。
試驗(yàn)中主要不良事件發(fā)生率為 2.9%�,精確單側(cè) 97.5%置信區(qū)間
上限為 5.7%,低于預(yù)先規(guī)定的12%性能目標(biāo)�����。共有 8 名受試者報(bào)告了 9 例主要不良事件�����,心包填塞/穿孔(3)�����、重大血管穿刺
并發(fā)癥/出血(2)�、心包炎(1)、卒中/腦血管意外(2)和短暫性腦缺血發(fā)作(1)�。所有受試者在隨訪結(jié)束前均達(dá)到已恢復(fù)/已緩解。未發(fā)生非預(yù)期器械不良反應(yīng)��。
如有醫(yī)療器械臨床試驗(yàn)設(shè)計(jì)服務(wù)需求�����,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò),聯(lián)系人:葉工��,電話:18058734169���,微信同。